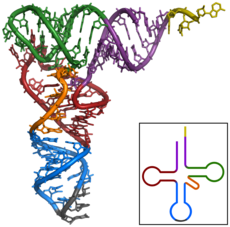
Биотехнология
Биотехноло́гия — дисциплина, изучающая возможности использования живых организмов, их систем или продуктов их жизнедеятельности для решения технологических задач, а также для возможности создания живых организмов с необходимыми свойствами методом генной инженерии.
Чаще всего применяется в медицине, пищевой промышленности, также для решение проблем в области энергетики, охране окружающей среды, и в научных исследованиях.
В последние десятилетия биология бурно развивается и создаёт новые научные направления. Новое комплексное направление — физико-химическая биология, включающая в себя биохимию, биофизику, молекулярные биологию и генетику, биоорганическую химию и некоторые другие дисциплины, — не только помогает решать задачи, которые давно ставила перед биологией производственно-техническая практика, но и намечает пути принципиально нового биологического производства.
В результате стремительного прогресса разных составных частей физико-химической биологии, возникло новое направление в науке и производстве, получившее наименование биотехнологии. Это направление сформировалось за последние два десятка лет и уже сейчас получило мощное развитие.
Особенно интенсивно биотехнология стала развиваться с 1981 года. Задачи физико-химической биологии очень обширны. Объединяет их то, что основу, суть каждой задачи составляет познание природы живого и использование в практике знаний о процессах и материальных структурах живых организмов. Стремительно расширяющиеся знания о процессах жизнедеятельности позволяют не только приспосабливать эти процессы для практических целей, но и управлять ими, а также создавать весьма перспективные в практическом отношении новые системы, не существующие в природе, хотя и аналогичные существующим.
Биотехнология в целом представляет собой систему приёмов направленного использования процессов жизнедеятельности живых организмов для получения промышленным способом ценных продуктов.
История биотехнологии[править | править код]

Отдельные элементы биотехнологии появились достаточно давно. По сути, это были попытки использовать в промышленном производстве отдельные клетки (микроорганизмы) и некоторые ферменты, способствующие протеканию ряда химических процессов.
Впервые термин «биотехнология» применил венгерский инженер Карл Эреки в 1917 году.
Использование в промышленном производстве микроорганизмов или их ферментов, обеспечивающих технологический процесс, известно издревле, однако систематизированные научные исследования позволили существенно расширить арсенал методов и средств биотехнологии.
Так, в 1814 году петербургский академик К. С. Кирхгоф открыл явление биологического катализа и пытался биокаталитическим путём получить сахар из доступного отечественного сырья (до середины XIX века сахар получали только из сахарного тростника). В 1891 году в США японский биохимик Дз. Такамине получил первый патент на использование ферментных препаратов в промышленных целях: учёный предложил применить диастазу для осахаривания растительных отходов.
В начале XX века активно развивалась бродильная и микробиологическая промышленность. В эти же годы были предприняты первые попытки использовать ферменты в текстильной промышленности.
В 1916—1917 годах русский биохимик А. М. Коленев пытался разработать способ, который позволил бы управлять действием ферментов в природном сырье при производстве табака.
Огромный вклад в дело практического использования достижений биохимии внёс академик А. Н. Бах, создавший важное прикладное направление биохимии — техническую биохимию. А. Н. Бах и его ученики разработали множество рекомендаций по улучшению технологий обработки самого различного биохимического сырья, совершенствованию технологий хлебопечения, пивоварения, виноделия, производства чая и табака и т. п., а также рекомендации по повышению урожая культурных растений путём управления протекающими в них биохимическими процессами.
Все эти исследования, а также прогресс химической и микробиологической промышленности и создание новых промышленных биохимических производств (чая, табака и т. п.) были важнейшими предпосылками возникновения современной биотехнологии.
В производственном отношении основой биотехнологии в процессе её формирования стала микробиологическая промышленность. За послевоенные годы микробиологическая промышленность приобрела принципиально новые черты: микроорганизмы стали использовать не только как средство повышения интенсивности биохимических процессов, но и как миниатюрные синтетические фабрики, способные синтезировать внутри своих клеток ценнейшие и сложнейшие химические соединения. Перелом был связан с открытием и началом производства антибиотиков.
Первый антибиотик — пенициллин — был выделен в 1940 году. Вслед за пенициллином были открыты и другие антибиотики (эта работа продолжается и поныне). С открытием антибиотиков сразу же появились новые задачи: налаживание производства лекарственных веществ, продуцируемых микроорганизмами, работа над удешевлением и повышением уровня доступности новых лекарств, получением их в очень больших количествах, необходимых медицине.
Синтезировать антибиотики химически было очень дорого или вообще невероятно трудно, почти невозможно (недаром химический синтез тетрациклина советским учёным академиком М. М. Шемякиным считается одним из крупнейших достижений органического синтеза). И тогда решили для промышленного производства лекарственных препаратов использовать микроорганизмы, синтезирующие пенициллин и другие антибиотики. Так возникло важнейшее направление биотехнологии, основанное на использовании процессов микробиологического синтеза.
Направления биотехнологии[править | править код]
Микробиологический синтез[править | править код]
Развитие микробиологической промышленности, выпускающей ценные продукты биосинтеза, позволило накопить очень важный опыт конструирования, производства и эксплуатации принципиально нового промышленного оборудования. Современное микробиологическое производство — производство очень высокой культуры. Технология его очень сложна и специфична, обслуживание аппаратуры требует овладения специальными навыками, ведь всё производство работает только в условиях строжайшей стерильности: стоит попасть в ферментатор лишь одной клетке микроорганизма другого вида, как всё производство может остановиться — «чужак» размножится и начнёт синтезировать совсем не то, что нужно человеку.
В настоящее время с помощью микробиологического синтеза производят антибиотики, ферменты, аминокислоты, полупродукты для дальнейшего синтеза разнообразных веществ, феромоны (вещества, с помощью которых можно управлять поведением насекомых), органические кислоты, кормовые белки и другие. Технология производства этих веществ хорошо отработана, получение их микробиологическим путём экономически выгодно.
В то же время идут поиски видов микроорганизмов, которые обладают способностью синтезировать в наибольших количествах другие необходимые вещества. В частности, учёные работают над тем, чтобы сделать выгодным производство с помощью микроорганизмов обычных химических продуктов: ацетона, различных спиртов, простых органических кислот, окиси пропилена и т. п. На микробиологической основе пытаются производить горючее: метан и спирт. Уже сейчас спирт, полученный микробиологическим путём, конкурирует с бензином по своим «рабочим» качествам, а также по показателям, очень важным с точки зрения охраны природы: продукты сгорания спирта не загрязняют окружающую среду.
Эти работы учёных важны ещё и по другой причине. Сейчас химическая промышленность для производства горючего, ацетона и других подобных веществ использует как исходное сырьё нефть, газ и уголь. Но их запасы не безграничны. А в микробиологической промышленности для производства химических продуктов могут использоваться (и уже частично используются) неограниченные, постоянно возобновляющиеся массы органического сырья, отходов, образующихся в сельском хозяйстве, лесной и деревообрабатывающей промышленности, очистных сооружениях городов и т. п. Разработка и внедрение эффективных технологий такого производства — задача, имеющая большое значение для экономики народного хозяйства.
Важным направлением биотехнологии является производство и использование так называемых иммобилизованных ферментов.
Использование ферментов — биологических катализаторов — очень заманчивая вещь. Ведь они по многим своим свойствам, прежде всего активности и избирательности действия (специфичности), намного превосходят катализаторы химические. Ферменты обеспечивают осуществление химических реакций без высоких температур и давлений, а ускоряют их в миллионы и миллиарды раз. При этом каждый фермент катализирует только одну определённую реакцию.
В пищевой и кондитерской промышленности ферменты применяются уже давно: многие из первых патентов ещё начала века касались производства ферментов именно для этих целей. Однако требования к этим препаратам тогда были не очень высокие — по существу, в производстве использовались не чистые ферменты, а различные вытяжки или полуразрушенные и высушенные клетки дрожжей или низших грибов. Ферменты (вернее, содержащие их препараты) использовали и в текстильной промышленности для отбеливания и обработки пряжи и хлопковых нитей (см. рис.1).
Биологические катализаторы можно использовать также не извлекая их из живых организмов, прямо в бактериальных клетках, например. Этот способ, собственно, есть основа всякого микробиологического производства, и применяется он издавна.
Гораздо заманчивее использовать чистые препараты ферментов и избавиться таким образом от побочных, сопутствующих жизнедеятельности микроорганизмов реакций. Создание производства, в котором используется биологический катализатор в чистом виде как реактив, сулит очень большие выгоды — повышается технологичность, возрастают во много тысяч раз производительность и чистота процессов. Но здесь возникает принципиальное затруднение: многие ферменты после их извлечения из клетки очень быстро инактивируются, разрушаются. Ни о каком многократном их использовании не может быть и речи.
Учёные нашли решение проблемы. Для того чтобы стабилизировать, или, как говорят, иммобилизовать, ферменты, сделать их устойчивыми, пригодными для многократного, длительного промышленного использования, ферменты присоединяют с помощью прочных химических связей к нерастворимым или растворимым носителям — ионообменным полимерам, полиорганосилоксанам, пористому стеклу, полисахаридам и т. п. В результате ферменты становятся устойчивыми и могут быть использованы многократно. (Эта идея была затем перенесена в микробиологию — возникла мысль иммобилизовать живые клетки. Иногда очень нужно, чтобы они в процессе микробиологического синтеза не загрязняли среду, не смешивались с синтезируемыми ими продуктами и вообще были бы больше похожи на химические реактивы. И такие иммобилизованные клетки были созданы; они успешно применяются, например, при синтезе стероидных гормонов — ценных лекарственных препаратов).
Разработка способа повышения устойчивости ферментов значительно расширяет возможности их использования. С помощью ферментов можно, например, получать сахар из растительных отходов, и этот процесс будет экономически рентабельным. Уже создана опытная установка для непрерывного производства сахара из клетчатки.
Иммобилизованные ферменты находят применение и в медицине. Так, в нашей стране для лечения сердечно-сосудистых заболеваний разработан препарат иммобилизованной стрептокиназы (препарат получил название «стрептодеказа»). Этот препарат можно вводить в сосуды для растворения образовавшихся в них тромбов. Растворимая в воде полисахаридная матрица (к классу полисахаридов относятся, как известно, крахмал и целлюлоза, близким к ним по строению был и подобранный полимерный носитель), к которой химически «привязана» стрептокиназа, значительно повышает устойчивость фермента, снижает его токсичность и аллергическое действие и не влияет на активность, способность фермента растворять тромбы.
Создание иммобилизованных ферментов, так называемая инженерная энзимология, — одно из новых направлений биотехнологий. Достигнуты лишь первые успехи. Но они существенно преобразили прикладную микробиологию, техническую биохимию и ферментную промышленность. Во-первых, в микробиологической промышленности сейчас актуальными стали разработки производства ферментов самой различной природы и свойства. Во-вторых, возникли новые области производства, связанные с получением именно иммобилизованных ферментов. В-третьих, создание новых ферментных препаратов открыло возможность организации ряда новых производств для получения нужных веществ с помощью биологические катализаторов.
Наномедицина[править | править код]
Слежение, исправление, конструирование и контроль над биологическими системами человека на молекулярном уровне, используя наноустройства и наноструктуры[1] В мире уже созданы ряд технологий для наномедицинской отрасли. К ним относятся адресная доставка лекарств к больным клеткам[2], лаборатории на чипе, новые бактерицидные средства.
Генная инженерия[править | править код]
Несмотря на то, что первые успешные опыты по трансформации клеток экзогенной ДНК были поставлены ещё в 1940-е года Эйвери, Маклеодом и Маккарти, первый коммерческий препарат человеческого рекомбинантного инсулина был получен только в 1970-е года. Введение чуждых для генома бактериальных клеток генов производят с использованием т. н. векторных ДНК, например плазмиды, присутствующие в бактериальных клетках, а также бактериофаги и другие мобильные генетические элементы могут быть использованы в качестве векторов для переноса экзогенной ДНК в клетку реципиента.
Получить новый ген можно:
- Вырезанием его из геномной ДНК хозяина при помощи рестрицирующей эндонуклеазы, катализирующей разрыв фосфодиэфирных связей между определёнными азотистыми основаниями в ДНК на участках с определённой последовательностью нуклеотидов;
- Химико-ферментативным синтезом;
- Синтезом кДНК на основе выделенной из клетки матричной РНК при помощи ферментов ревертазы и ДНК-полимеразы, при этом изолируется ген, не содержащий незначащих последовательностей и способный экспрессироваться при условии подбора подходящей промоторной последовательности в прокариотических системах без последующих модификаций, что чаще всего необходимо при трансформации прокариотических систем эукариотическими генами, содержащими интроны и экзоны.
После этого обрабатывают векторную молекулу ДНК рестриктазой с целью образования двуцепочечного разрыва и в образовавшуюся «брешь» производится «вклеивание» гена в вектор используя фермент ДНК-лигазу, а затем такими рекомбинантными молекулами трансформируют клетки реципиента, например клетки кишечной палочки. При трансформации с использованием в качестве вектора, например, плазмидной ДНК необходимо, чтобы клетки были компетентными для проникновения экзогенной ДНК в клетку, для чего например используют электропорацию клеток реципиента. После успешного проникновения в клетку экзогенная ДНК начинает реплицироваться и экспрессироваться в клетке.
Плазмиды[править | править код]
Наибольшие успехи были достигнуты в области изменения генетического аппарата бактерий. Вводить новые гены в геном бактерии научились с помощью небольших кольцеобразных молекул ДНК — плазмид, присутствующих в бактериальных клетках. В плазмиды «вклеивают» необходимые гены, а затем такие гибридные плазмиды добавляют к культуре бактерий, например кишечной палочки. Некоторые из этих бактерий поглощают такие плазмиды целиком. После этого плазмида начинает работать в клетке как ген, изготавливая в клетке кишечной палочки десятки своих копий, которые обеспечивают синтез новых белков.
Клеточная инженерия[править | править код]
Сейчас созданы и создаются ещё более остроумные методы введения генов в клетку прокариотов (организмов, не имеющих оформленного ядра и хромосомного аппарата). На очереди разработка методов введения новых генов в клетки эукариотов, прежде всего высших растений и животных организмов.
Но и то, что уже достигнуто, позволяет сделать очень многое в практике народного хозяйства. Возможности микробиологического производства значительно расширились. Благодаря генетической инженерии область микробиологического синтеза различных биологически активных соединений, полупродуктов для синтеза, кормовых белков и добавок и других веществ стала одной из наиболее окупаемых наук: вложение средств в перспективные биотехнологические исследования обещает получение высокого экономического эффекта.
Для селекционной работы, независимо от того, проводится она методами мутагенеза или «индустрии ДНК», учёные должны располагать многочисленными коллекциями микроорганизмов. Но сейчас даже выделение нового штамма природных микроорганизмов, ранее неизвестных науке, обходится на мировом «рынке бактериальных культур» приблизительно в 100 долларов. А для того, чтобы получить хороший промышленный штамм обычными селекционными методами, надо иногда затратить миллионы.
Сейчас уже существуют способы ускорить и удешивить эти процессы. Например, во Всесоюзном научно-исследовательском институте генетики и селекции микроорганизмов Главмикробиопрома был получен промышленный штамм-сверхпродуцент микроорганизма, синтезирующего треонин — незаменимую аминокислоту, которая в кормах сельскохозяйственных животных содержится в недостаточном количестве. Добавка треонина в корм повышает привесы животных на килограммы, что в масштабах страны оборачивается миллионами рублей прибыли, а самое главное — приростом мясной продукции животноводства.
Коллектив учёных института под руководством директора В. Г. Дебабова за основу для получения промышленного штамма взял обыкновенную кишечную палочку — повсеместно распространённый микроорганизм. Сначала были получены мутантные клетки, способные накапливать в среде избыток треонина. Затем в клетке были вызваны генетические изменения, которые привели к усилению биосинтеза аминокислот. Таким путём удалось получить штамм, который производил треонин, но в 10 раз меньше того количества, которое требовалось по соображениям рентабельности производства. Тогда в дело были выпущены методы генетической инженерии. С их помощью была увеличена «доза треонинового гена» в молекуле бактериальной ДНК. Причём количество генов, обусловливающих синтез треонина, было в молекуле ДНК клетки увеличено в несколько раз: одинаковые гены оказались как бы нанизанными один за другим в молекуле ДНК. Естественно, биосинтез треонина пропорционально увеличился и достиг уровня, достаточного для промышленного производства.
Правда, после этого штамм пришлось ещё улучшать, причём снова генетически. Сначала для того, чтобы культуру бактерий очистить от клеток, в которых плазмиды с «треониновым геном» исчезали в процессе размножения культуры. Для этого в клетки был «вшит» ген, содержащий закодированный сигнал к «самоубийству» клеток, в которых плазмид с «треониновым геном» после деления не оказывалось. Таким путём культура клеток самоочищалась от балластных микроорганизмов. Затем в клетки был введён ген, благодаря которому она могла развиваться на сахарозе (а не дорогих глюкозе и фруктозе, как раньше) и производить рекордные количества треонина.
По существу, полученный микроорганизм уже не был кишечной палочкой: манипуляции с его генетическим аппаратом привели к появлению принципиально нового организма, сконструированного вполне сознательно и целенаправленно. И эта сложнейшая многоступенчатая работа, имеющая огромное практическое значение, была проведена с помощью новых оригинальных методов генетической инженерии за очень короткий срок — всего за три года.
К 1981 г. в ряде институтов страны, и прежде всего в Институте биоорганической химии им. М. М. Шемякина АН СССР под руководством академика Ю. А. Овчиникова, были выполнены ещё более впечатляющие работы. Эти исследования приобрели сейчас форму чётких долгосрочных программ, по которым их развивают дальше ряд академических и отраслевых институтов. Эти исследования были направлены на то, чтобы осуществить поистине чудо — ввести в бактериальную клетку ген, выделенный из человеческого организма.
Работа велась сразу с несколькими генами: геном ответственным за синтез гормона инсулина, геном, обеспечивающим образование интерферона, и геном, контролирующим синтез гормона роста.
Прежде всего учёные поставили перед собой задачу «обучения» бактерии синтезу ценнейшего медицинского препарата — гормона инсулина.
Инсулин необходим для лечения сахарного диабета. Этот гормон надо вводить больным постоянно, а производство его традиционным способом (из поджелудочных желез убойного скота) сложно и дорого. К тому же молекулы инсулина свиньи или крупного рогатого скота отличаются от молекул инсулина человека, и естественно, что активность их в организме человека ниже, чем активность человеческого инсулина. Кроме того, инсулин — хотя и небольшой по размерам, но всё же белок, и в организме человека со временем накапливаются антитела к нему: организм борется против чужеродных белков, отторгает их. Поэтому введённый бычий или свиной инсулин может начать необратимо инактивироваться, нейтрализовываться этими антителами и в результате может исчезнуть прежде, чем успеет оказать лечебное действие. Чтобы этого не произошло, необходимо вводить в организм вещества, предотвращающие этот процесс, но они сами по себе не безразличны для организма.
Человеческий инсулин можно было бы получать с помощью химического синтеза. Но этот синтез настолько сложен и дорог, что его проводили только в экспериментальных целях, а полученные количества инсулина были недостаточны даже для одной инъекции. Это был, скорее, символической синтез, доказательство того, что химики могут синтезировать в пробирке настоящий белок.
Учитывая всё это, учёные и поставили перед собой такую сложную и очень важную задачу — наладить биохимическое производство человеческого инсулина. Был получен ген, обеспечивающий синтез инсулина. С помощью методов генетической инженерии этот ген был введён в бактериальную клетку, которая в результате приобрела способность синтезировать гормон человека.
Столь же большой интерес и не меньшее (а может быть, и большее) значение имела работа, выполненная в том же институте, по введению методами генетической инженерии в бактериальную клетку гена, ответственного за синтез интерферона человека. (Интерферон — это белок, играющий исключительно важную роль в борьбе организма против вирусных инфекций.) Ген интерферона также был введён в клетку кишечной палочки. Созданные штаммы отличались высоким выходом интерферона, обладающего мощным противовирусным действием. Сейчас уже получены первые промышленные партии человеческого интерферона. Осуществление промышленного производства интерферона — очень важное достижение, так как предполагают, что интерферон обладает также и противоопухолевой активностью.
В институте АН СССР были проведены работы по созданию бактериальных клеток, продуцирующих соматотропин — гормон роста человека. Ген этого гормона был выделен из гипофиза и методами генетической инженерии встроен в более сложную молекулу ДНК, которую затем ввели в генетический аппарат бактерии. В результате бактерия приобрела способность синтезировать человеческий гормон. Эта бактериальная культура, так же как и культура бактерий с введённым геном инсулина, апробируется для промышленного получения человеческих гормонов в микробиологическом производстве.
Это лишь отдельные примеры работ по введению генов высших организмов в клетки бактерий. Есть ещё немало подобных интересных и перспективных работ.
Вот ещё один пример. Английские биохимики из плодов одного африканского кустарника выделили довольно крупный белок (около 200 аминокислотных остатков) — тауматин. Этот белок оказался в 100 тыс. раз слаще сахарозы. Сейчас во всём мире думают над созданием заменителей сахара, который при большом потреблении далеко не безвреден для организма. Поэтому тауматин — природный продукт, не требующий специальных токсикологических испытаний, — привлёк пристальное внимание: ведь ничтожные его добавки в кондитерские изделия позволяют просто исключить использование сахара. Учёные решили, что получать тауматин проще и выгоднее не из естественного источника, а микробиологическим синтезом с помощью бактерий, в которые введён ген тауматина. И эту работу выполнили, введя этот ген во всё ту же кишечную палочку. Сейчас пока заменитель сахара тауматин (под названием «талин») производят из природного источника, но не за горами и его микробиологическое производство.
Пока речь шла о введении генов в клетки бактерий. Но это не означает, что не ведётся работа и по введению искусственных генов в высшие организмы — растения и животных. Здесь не меньше, а гораздо больше привлекательных идей. Практическое воплощение некоторых из них будет иметь для человечества исключительно важное значение. Так, известно, что высшие растения не могут усваивать азот атмосферы: они получают его из почвы в виде неорганических солей или в результате симбиоза с клубеньковыми бактериями. Осуществление идеи — ввести гены этих бактерий в растения — может привести к коренным революционным изменениям в сельском хозяйстве.
Как же обстоят дела с введением генов в генетический аппарат эукариотов? Основная трудность здесь заключается в том, что изменить генотип всех клеток многоклеточного организма невозможно. Поэтому надежды связывают с созданием методов генетической инженерии, предназначенных для работы с культурами клеток растений и с одноклеточными растениями.
Введение синтетических генов в искусственно культивируемые клетки может привести к получению модифицированного растения: при определённых условиях изолированные клетки могут превращаться в целые растения. И в таком растении должны действовать и передаваться по наследству искусственно введённые в исходную клетку гены.
Здесь помимо перспектив успешного использования методов генетической инженерии вырисовывается ещё одно преимущество биотехнологии — методом клеточной биотехнологии из одного растения можно получить миллионы одинаковых растений, а не десятки, как при использовании семян. Клеточная технология не требует больших площадей, не зависит от погодных условий и отличается огромной производительностью.
Советские учёные сейчас исследуют ещё один путь введения генов в клетки растений — создают симбиотическое сообщество, где в протопласты растений (они лишены целлюлозной оболочки) пытаются внедрить цианобактерии, которые способны и к фотосинтезу, и к азотфиксации.
Определённые перспективы имеются и в области использования методов генетической инженерии в работе с животными, во всяком случае существует принципиальная возможность переноса генетического материала в клетки животных. Особенно убедительно это показано на гибридомах. Гибридома — это клетка, образованная из лимфоцита, вырабатывающего антитела, и опухолевой клетки, способной к неограниченному размножению, и сочетающая оба эти свойства. С помощь гибридом можно получать высокоспецифичные антитела. Метод гибридом — это ещё один биотехнологический приём получения ценных белков.
Биогеотехнология[править | править код]
Данное направление было ранее известно как Микробное выщелачивание металлов из руд. Изучает добычу металлов из их руд при помощи микроорганизмов. В 50-е — 60-е годы выяснилось, что существуют микроорганизмы, способные переводить металлы из рудных минералов в раствор. Механизмы такого перевода бывают разные. Например, некоторые выщелачивающие микроорганизмы непосредственно окислют пирит:
А ион трехвалентного железа служит сильным окислющим агентом, способным перевести в растовор Медь из халькоцинита: или Уран из уранинита:
Реакции окисления являются экзормическими, при их протекании выделяется энергия, используемая микроогранизмами в ходе своей жизнедеятельности.
Итак, какова же структура биотехнологии? Учитывая, что биотехнология активно развивается и структура её окончательно не определилась, можно говорить лишь о тех видах биотехнологии, которые существуют в настоящее время. Это клеточная биотехнология — прикладная микробиология, культуры растительных и животных клеток (об этом шла речь, когда мы говорили о микробиологической промышленности, о возможностях клеточных культур, о химическом мутагенезе). Это генетическая биотехнология и молекулярная биотехнология (они обеспечивают «индустрию ДНК»). И наконец, это моделирование сложных биологических процессов и систем, включающее инженерную энзимологию (об этом мы говорили, когда рассказывали об иммобилизованных ферментах).
Очевидно, что биотехнология имеет огромное будущее. И дальнейшее её развитие тесно связано с одновременным развитием всех важнейших отраслей биологической науки, исследующих живые организмы на разных уровнях их организации. Ведь как бы ни дифференцировалась биология, какие бы новые научные направления не возникали, объектом их исследования всегда будут живые организмы, представляющие собой совокупность материальных структур и разнообразнейших процессов составляющих физическое, химическое и биологическое единство. И этим — самой природой живого — предопределяется необходимость комплексного изучения живых организмов. Поэтому естественно и закономерно что биотехнология возникла в результате прогресса комплексного направления — физико-химической биологии и развивается одновременно и параллельно с этим направлением.
Всегда одной из основных практических задач клеточной и тканевой инженерии являлось создание на основе культивированных in vitro клеток живых эквивалентов тканей и органов с целью их использования в заместительной терапии для восстановления повреждённых структур и функций организма. Наибольшие успехи в этом направлении достигнуты при использовании выращенных in vitro кератиноцитов для лечения повреждений кожного покрова, и в первую очередь — при лечении ожоговых ран.
В заключение надо отметить ещё одно важное обстоятельство, которое отличает биотехнологию от других направлений науки и производства. Она исходно ориентирована на проблемы, которые тревожат современное человечество: производство продуктов питания (прежде всего белка), сохранение энергетического равновесия в природе (отход от ориентировки на использование невосполнимых ресурсов в пользу ресурсов восполнимых), охрана окружающей среды (биотехнология — «чистое» производство, требующее, правда, больших затрат воды).
Таким образом, биотехнология — закономерный результат развития человечества, признак достижения им важного, можно сказать поворотного, этапа развития.
Биотехнологическая промышленность[править | править код]
Биотехнологическую промышленность иногда разделяют на четыре направления:
- «Красная» биотехнология — производство биофармацевтических препаратов (протеинов, ферментов, антител) для человека, а также коррекция генетического кода.
- «Зелёная» биотехнология — разработка и внедрение в культуру генетически модифицированных растений.
- «Белая» биотехнология — производство биотоплив, ферментов и биоматериалов для различных отраслей промышленности.
- Академические и правительственные исследования — например, расшифровка генома риса.
Микробиологическая индустрия выпускает 150 видов продукции, крайне необходимой народному хозяйству. Её гордость — кормовой белок, получаемый на основе выращивания дрожжей. В год его производят более 1 млн тонн. Другое важное достижение — выпуск ценнейшей кормовой добавки — незаменимой (то есть не образующейся в организме животного) аминокислоты лизина. Усвояемость белковых веществ, содержащихся в продукции микробиологического синтеза, такова, что 1 т кормового белка экономит 5‒8 т зёрна. Добавка 1 т биомассы дрожжей в рацион птиц, например, позволяет получить дополнительно 1,5‒2 т мяса или 25‒35 тыс. яиц, а в свиноводстве — высвободить 5‒7 т фуражного зёрна. Дрожжи — не единственный возможный источник белка. Он может быть получен путём выращивания микроскопических зелёных водорослей, различных простейших и других микроорганизмов. Уже разработаны технологии их использования, проектируются и строятся предприятия-гиганты мощностью от 50 до 300 тыс. тонн продукции в год. Их эксплуатация позволит внести весомый вклад в решение народно-хозяйственных задач.
Если ген человека, отвечающий за синтез какого-либо фермента или другого важного для организма вещества, пересадить в клетки микроорганизмов, то в соответствующих условиях микроорганизмы будут продуцировать чуждое им соединение в промышленных масштабах. Учёные разработали и внедрили в производство способ получения интерферона человека эффективного при лечении многих вирусных заболеваний. Из 1 л культуральной жидкости извлекают такое же количество интерферона, какое раньше получали из многих тонн донорской крови. Экономия от внедрения нового способа составляет 200 млн рублей в год.
Другой пример — получение с помощью микроорганизмов гормона роста человека. Совместные разработки учёных Института молекулярной биологии, Института молекулярной биологии, Института биохимии и физиологии микроорганизмов России и институтов России позволяют производить уже граммы гормона, тогда как прежде этот препарат получали миллиграммами. В настоящее время препарат проходит испытания. Методы генетической инженерии создали возможность получения вакцин против таких опасных инфекций, как гепатит В, ящур крупного рогатого скота, а также разработки способов ранней диагностики ряда наследственных заболеваний и различных вирусных инфекций.
Генетическая инженерия начинает активно воздействовать на развитие не только медицины, но и других сфер народного хозяйства. Успешное развитие методов генетической инженерии открывает широкие возможности для решения ряда задач, стоящих перед сельским хозяйством. Это и создание новых ценных сортов сельскохозяйственных растений, устойчивых к различным заболеваниям и неблагоприятным факторам внешней среды, и ускорение процесса селекции при выведении высокопродуктивных пород животных, и создание для ветеринарии высокоэффективных средств диагностики и вакцин, и разработка методов биологической фиксации азота. Решение этих проблем будет способствовать научно-техническому прогрессу сельского хозяйства, и ключевая роль в этом будет принадлежать методам генетической, а также, очевидно, и клеточной инженерии.
Клеточная инженерия — необычайно перспективное направление современной биотехнологии. Учёные разработали методы выращивания в искусственных условиях (культивирование) клеток растений животных и даже человека. Культивирование клеток позволяет получать различные ценные продукты, ранее добываемые в очень ограниченном количестве из-за отсутствия источников сырья. Особенно успешно развивается клеточная инженерия растений. Используя методы генетики, удаётся отбирать линии таких клеток растений — продуцентов практически важных веществ, которые способны расти на простых питательных средах и в то же время накапливать ценных продуктов в несколько раз больше, чем само растение. Выращивание массы клеток растений уже используется в промышленных масштабах для получения физиологически активных соединений. Налажено, например, производство биомассы женьшеня для нужд парфюмерной и медицинской промышленности. Закладываются основы производства биомассы лекарственных растений — диоскореи и раувольфии. Разрабатываются способы выращивания клеточной массы других редких растений — продуцентов ценных веществ (родиолы розовой и др.). Другое важное направление клеточной инженерии — клональное микроразмножение растений на основе культуры тканей. Основан это метод на удивительном свойстве растений: из отдельной клетки или кусочка ткани в определённых условиях может вырасти целое растение, способное к нормальному росту и размножению. Этим методом из небольшой части растения можно получить до 1 млн растений в год. Клональное микроразмножение используется для оздоровления и быстрого размножения редких, хозяйственно ценных или вновь созданных сортов сельскохозяйственных культур. Таким путём из клеток, не заражённых вирусами, получают здоровые растения картофеля, винограда, сахарной свёклы, садовой земляники, малины и многих других культур. В настоящее время разработаны методы микроразмножения и более сложных объектов — древесных растений (яблони, ели, сосны). На основе этих методов будут созданы технологии промышленного получения исходного посадочного материала ценных древесных пород. Методы клеточной инженерии позволят значительно ускорить селекционный процесс при выведении новых сортов хлебных злаков и других важных сельскохозяйственных культур: срок их получения сокращается до 3‒4 лет (вместо 10‒12 лет, необходимых при использовании обычных методов селекции). Перспективных способом выведения новых сортов ценных сельскохозяйственных культур является также разработанный учёными принципиально новый метод слияния клеток. Этот метод позволяет получать гибриды, которые не могут быть созданы обычным путём скрещивания в силу барьера межвидовой несовместимости. Методом слияния клеток получены, например, гибриды различных видов картофеля, томатов, табака; табака и картофеля, рапса и турнепса, табака и белладонны. На основе гибрида культурного и дикого картофеля, который устойчив к вирусам и другим заболеваниям, создаются новые сорта. Аналогичным способом получают ценный селекционный материал томатов и других культур. В перспективе — комплексное использование методов генетической и клеточной инженерии для создания новых сортов растений с заранее заданными свойствами, например, ос сконструированными в них системами фиксации атмосферного азота. Большие успехи достигнуты клеточной инженерией в области иммунологии: разработаны методы получения особых гибридных клеток, производящих индивидуальные, или моноклональные, антитела. Это позволило создать высокочувствительные средства диагностики ряда тяжёлых заболеваний человека, животных и растений. Значительный вклад вносит современная биотехнология в решение такой важной проблемы, как борьба с вирусными заболеваниями сельскохозяйственных культур, наносящими большой ущерб народному хозяйству. Учёные разработали высокоспецифичные сыворотки для выявления более 20 вирусов, вызывающих заболевания различных сельскохозяйственных культур. Разработана и изготовлена система приборов и приспособлений для массовой автоматической экспресс-диагностики вирусных болезней растений в условиях сельскохозяйственного производства. Новые методы диагностики позволяют отбирать для посадки свободный от вирусов исходный материал (семена, клубни и др.), что способствует значительному повышению урожая. Важное практическое значение имеют работы по инженерной энзимологии. Первым важным успехом её была иммобилизация ферментов — закрепление молекул ферментов с помощью прочных химических связей на синтетических полимерах, полисахаридах и других носителях-матрицах. Закреплённые ферменты более стабильны, их можно использовать многократно. Иммобилизация позволяет осуществлять непрерывные каталитические процессы, получать продукцию, не загрязнённую ферментом (что особенно важно в ряде пищевых и фармакологических производств), значительно снизить её себестоимость. Это метод применяют, например, для получения антибиотиков. Так, учёными разработана и внедрена в промышленное производство технология получения антибиотиков на основе иммобилизованного фермента пенициллинамидазы. В результате применения этой технологии в пять раз снизился расход сырья, себестоимость конечного продукта уменьшилась почти вдвое, объём производства возрос в семь раз, а общий экономический эффект составил около 100 млн рублей. Следующим шагом инженерной энзимологии была разработка методов иммобилизации клеток микроорганизмов, а затем — клеток растений и животных. Иммобилизованные клетки являются наиболее экономичными биокатализаторами, так как обладают высокой активностью и стабильностью, а главное — применение их полностью исключает затраты на выделение и очистку ферментов. В настоящее время на основе иммобилизованных клеток разработаны методы получения органических кислот, аминокислот, антибиотиков, стероидов, спиртов и других ценных продуктов. Иммобилизованные клетки микроорганизмов используются также для очистки сточных вод, переработки сельскохозяйственных и промышленных отходов. Биотехнология находит всё более широкое применение и во многих отраслях промышленного производства: разработаны методы использования микроорганизмов для извлечения цветных благородных металлов из руд и промышленных отходов, для повышения нефтеотдачи пластов, для борьбы с метаном в угольных шахтах. Так, для освобождения шахт от метана учёные предложили бурить скважины в угольных пластах и подавать в них суспензию из метаноокисляющихся бактерий. Таким образом удаётся удалить около 60 % метана ещё до начала эксплуатации пласта. А недавно нашли более простой и эффективный способ: суспензией из бактерий опрыскивают породы выработанного пространства, откуда наиболее интенсивно выделяется газ. Разбрызгивание суспензии можно осуществлять с помощью специальных форсунок, устанавливаемых на крепях. Испытания, которые были проведены на шахтах Донбасса, показали, что микроскопические «работники» быстро уничтожают от 50 до 80 % опасного газа в выработках. А вот с помощью других бактерий, которые сами выделяют метан, можно повышать давление в нефтяных пластах и обеспечивать более полное извлечение нефти. Значительный вклад предстоит внести биотехнологии и в решение энергетической проблемы. Ограниченность запасов нефти и газа заставляет искать пути использования нетрадиционных источников энергии. Один из таких путей — биоконверсия растительного сырья, или, другими словами, ферментативная переработка целлюлозосодержащих отходов промышленности и сельского хозяйства. В результате биоконверсии можно получить глюкозу, а из неё — спирт, который и будет служить топливом. Всё шире развёртываются исследования по получению биогаза (в основном метана) путём переработки животноводческих, промышленных и коммунальных отходов с помощью микроорганизмов. При этом остатки после переработки являются высокоэффективным органическим удобрением. Таким образом, этим путём решаются сразу несколько проблем: охрана окружающей среды от загрязнений, получение энергии и производство удобрений. Установки по получению биогаза уже работают в разных странах. Возможности биотехнологии практически безграничны. Она смело вторгается в самые разные сферы народного хозяйства. И в недалёком будущем, несомненно, ещё более возрастёт практическая значимость биотехнологии в решении важнейших задач селекции, медицины, энергетики, охраны окружающей среды от загрязнений.
Трансгенные растения[править | править код]
Трансгенные растения — это те растения, которым пересажены гены.
- 1. Картофель устойчивый к колорадскому жуку, был создан путём введения гена выделенный из ДНК клетки почвенной тюрингской бациллы, вырабатывающий белок, ядовитый для колорадского жука (в желудке жука вырабатывается яд, а в человеке нет). Использовали посредника — клетки кишечной палочки. Листья картофеля стали вырабатывать белок, ядовитый для жуков.
- 2. Использует продукты из трансгенной сои, кукурузы, картофеля и подсолнечника.
- 3. В Америке решили вырастить помидор устойчивый к заморозкам. Взяли ген камбалы, отвечающий за терморегуляцию, и пересадили в клетки томата. Но помидор эту информацию понял по-своему, он не перестал бояться заморозков, а перестал портиться при хранении. Он может полгода лежать в комнате и не гнить.
Картофель, устойчивый к колорадскому жуку, был создан путём введения гена выделенного из генома почвенной тюрингской бациллы Bacillus thuringiensis, вырабатывающий белок Cry, представляющий собой протоксин, в кишечнике насекомых этот белок растворяется и активируется до истинного токсина, губительно действующего на личинок и имаго насекомых, у человека и других теплокровных животных подобная трансформация протоксина невозможна и соответственно этот белок для человека не токсичен и безопасен. Опрыскивание спорами Bacillus thuringiensis использовалось для защиты растений и до получения первого трансгенного растения, но с низкой эффективностью, продукция эндотоксина внутри тканей растения существенно повысило эффективность защиты, а также повысило экономическую эффективность ввиду того что растение само начало продуцировать защитный белок. Путём трансформации растения картофеля при помощи Agrobacterium tumefaciens были получены растения, синтезирующие этот белок в мезофилле листа и других тканях растения и соответственно непоражаемые колорадским жуком. Данный подход используется и для создания других сельскохозяйственных растений, резистентных к различным видам насекомых.
Оценка безопасности трансгенных растений[править | править код]
Самым современным тестом, позволяющим оценить безопасность трансгенных растений на органы и системы человека является экологический тест ЭКОТЕМ©® разработанный российскими учеными-экологами биоремедиации Есиной Е. А. и Мусиным М.Н. Экологический тест ЭКОТЕМ©® применяется для оценки возможного воздействия на позволяет получить в цифровом выражении воздействия комплексной смеси веществ, биомассы растений и т. д. (без деления на составляющие) на органы и системы человека. таких, как пинеальная железа, миндалины, лимфоглоточное кольцо, легкие, толстый кишечник, центральная нервная система, периферическая нервная система, сердце и органы кровообращения, кроветворная система, 12-перстная кишка, поджелудочная железа, печень, почки, мочевой пузырь, урогенитальные органы, желчевыводящая система, кожные покровы, суставы и позвоночник.
Экологический тест ЭКОТЕМ©® применяется во всероссийском конкурсе Одобрения Экологами России и присвоения товарного знака Одобрения экологами Российской Федерации
Трансгенные животные[править | править код]
Трансгенные животные, экспериментально полученные животные, содержащие во всех клетках своего организма дополнительную интегрированную с хромосомами и экспрессирующуюся чужеродную ДНК (трансген), которая передаётся по наследству по законам Менделя.
Изредка трансген может реплицироваться и передаваться по наследству как экстрахромосомный автономно реплицирующийся фрагмент ДНК. Термин «трансгеноз» был предложен в 1973 для обозначения переноса генов одних организмов в клетки организмов других видов, в том числе далёких в эволюционном отношении. Получение трансгенных животных осуществляется с помощью переноса клонированных генов (ДНК) в ядра оплодотворенных яйцеклеток (зигот) или эмбриональных стволовых (плюрипотентных) клеток. Затем в репродуктивные органы реципиентной самки пересаживают модифицированные зиготы или яйцеклетки, у которых собственное ядро заменено на модифицированное ядро эмбриональных стволовых клеток, либо бластоцисты (эмбрионы), содержащие чужеродную ДНК эмбриональных стволовых клеток. Имеются отдельные сообщения об использовании спермиев для создания трансгенных животных, однако этот приём пока не получил широкого распространения.
Первые трансгенные животные были получены в 1974 в Кембридже (США) Рудольфом Янишем (Jaenisch) в результате инъекции в эмбрион мыши ДНК вируса обезьяны SV40. В 1980 американским учёным Жоржем Гордоном (Gordon) с соавторами было предложено использовать для создания трансгенных животных микроинъекцию ДНК в пронуклеус зиготы. Именно этот подход положил начало широкому распространению технологии получения трансгенных животных. Первые трансгенные животные в России появились в 1982. С помощью микроинъекций в пронуклеус зиготы в 1985 в США были получены первые трансгенные сельскохозяйственные животные (кролик, овца, свинья). В настоящее время для создания трансгенных животных, кроме микроинъекций, используются другие экспериментальные приемы: инфицирование клеток рекомбинантными вирусами, электропорация, «обстрел» клеток металлическими частицами с нанесёнными на их поверхности рекомбинантными ДНК.
В последние годы в результате появления технологии клонирования животных возникли дополнительные возможности для создания трансгенных животных. Уже есть трансгенные животные, полученные с помощью микроинъекции генов в ядра дифференциированных клеток.
Все имеющиеся методы переноса генов пока ещё не очень эффективны. Для получения одного трансгенного животного в среднем необходимы микроинъекции ДНК в 40 зигот мышей, 90 зигот козы, 100 зигот свиньи, 110 зигот овцы и в 1600 зигот коровы. Механизмы интеграции экзогенной ДНК или формирования автономных репликонов (единиц репликации, отличных от хромосом) при трансгенозе не известны. Встраивание трансгенов у каждого вновь получаемого трансгенного животного происходит в случайные участки хромосом, причём может происходить встраивание как единичной копии трансгена, так и множества копий, располагающихся, как правило, тандемно в единичном локусе одной из хромосом. Как правило, гомология между сайтом (местом) интеграции трансгена и самим трансгеном отсутствует. При использовании для трансгеноза эмбриональных стволовых клеток возможна предварительная селекция, что позволяет получать трансгенных животных с трансгеном, интегрированным в результате гомологичной рекомбинации с определённым участком генома хозяйского организма. С помощью этого подхода осуществляют, в частности, целенаправленное прекращение экспрессии определённого гена (это называют «нокаутом гена»).
Технология создания трансгенных животных является одной из наиболее бурно развивающихся биотехнологий в последние 10 лет. Трансгенные животные широко используются как для решения большого числа теоретических задач, так и в практических целях для биомедицины и сельского хозяйства. Некоторые научные проблемы не могли бы быть решены без создания трансгенных животных. На модели трансгенных лабораторных животных проводятся широкие исследования по изучению функции различных генов, регуляции их экспрессии, фенотипическому проявлению генов, инсерционному мутагенезу и др. Трансгенные животные важны для различных биомедицинских исследований. Существует множество трансгенных животных, моделирующих различные заболевания человека (рак, атеросклероз, ожирение и др.). Так, получение трансгенных свиней с изменённой экспрессией генов, определяющих отторжение органов, позволит использовать этих животных для ксенотрансплантации (пересадки органов свиньи человеку). В практических целях трансгенные животные используются различными зарубежными фирмами как коммерческие биореакторы, обеспечивающие производство разнообразных медицинских препаратов (антибиотиков, факторов свёртываемости крови и др.). Кроме того, перенос новых генов позволяет получать трансгенных животных, отличающихся повышенными продуктивными свойствами (например, усиление роста шерсти у овец, понижение содержания жировой ткани у свиней, изменение свойств молока) или устойчивостью к различным заболеваниям, вызываемым вирусами и другими патогенами. В настоящее время человечество уже использует множество продуктов, получаемых с помощью трансгенных животных: медицинские препараты, органы, пища.
Клонирование животных[править | править код]
См. статью Клонирование животных и растений.
См. также[править | править код]
- Генная инженерия
- Трансгены
- Биокомпьютер Эдлмана
- Конечный биоавтомат Шапиро
- Ксенотрансплантация
- Биопанк
- Нанотехнология
Примечания[править | править код]
- ↑ Nanomedicine, Volume I: Basic Capabilities, by Robert A. Freitas Jr. 1999, ISBN 157059645X
- ↑ LaVan DA, McGuire T, Langer R. (2003). "Small-scale systems for in vivo drug delivery". Nat Biotechnol 21 (10): 1184–1191. DOI:10.1038/nbt876.